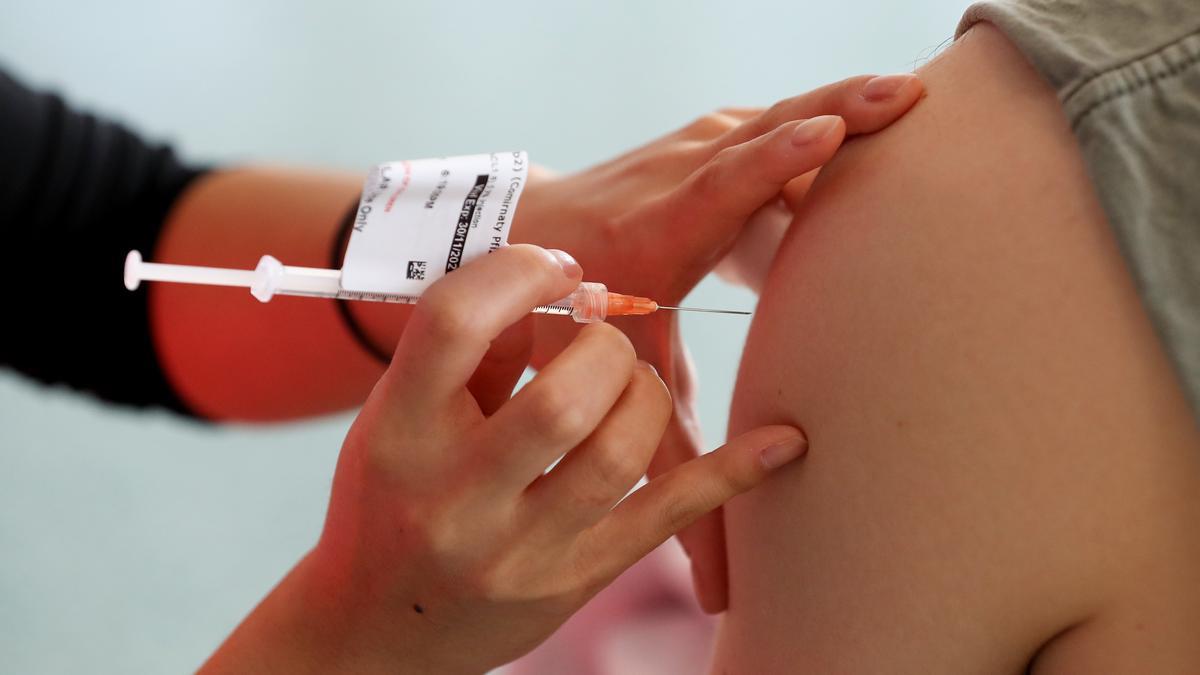
La Agencia Europea del Medicamento (EMA, por sus siglas en inglés) ha comenzado a evaluar una solicitud para ampliar el uso de la vacuna contra la COVID-19 de BioNTech/Pfizer a niños de 5 a 11 años.
El Comité de Medicamentos de Uso Humano (CHMP, por sus siglas en inlgés) de la EMA revisará los datos sobre la vacuna, incluidos los resultados de un estudio clínico en curso en el que participan niños de entre 5 y 11 años, para decidir si recomienda ampliar su uso.
El dictamen del CHMP se remitirá a la Comisión Europea, que emitirá una decisión final. La EMA comunicará el resultado de su evaluación "en un par de meses, a menos que se necesite información adicional".
Esta vacuna está actualmente autorizada para su uso en personas de 12 años o más. Contiene una molécula llamada ARN mensajero (ARNm) con instrucciones para producir una proteína, conocida como proteína de espiga, que está presente de forma natural en el SARS-CoV-2, el virus que causa la COVID-19. La vacuna actúa preparando al organismo para defenderse del SARS-CoV-2.
Nueva fórmula para Pfizer
Por su parte, el Comité de Medicamentos de Uso Humano (CHMP, por sus siglas en inglés) de la Agencia Europea del Medicamento (EMA, por sus siglas en inglés) ha aprobado dos nuevos centros de fabricación para la producción de la vacuna contra la COVID-19 de BioNTech y Pfizer.
Uno de los centros, situado en Monza (Italia), está gestionado por Patheon Italia. El otro, situado en Anagni, también en Italia, está gestionado por Catalent Anagni. Ambos centros fabricarán el producto acabado. Estos centros producirán hasta 85 millones de dosis adicionales para abastecer a la UE en 2021.
Estas recomendaciones no requieren una decisión de la Comisión Europea, por lo que los centros pueden entrar en funcionamiento "inmediatamente".
Por otra parte, el CHMP ha aprobado una formulación de la vacuna contra la COVID-19 de BioNTech y Pfizer lista para usar. Esta formulación no requiere dilución antes de la administración, estará disponible en un tamaño de envase de 10 viales (60 dosis) y puede almacenarse a 2-8°C durante un máximo de 10 semanas.
La formulación concentrada actual requiere dilución antes de la administración, está disponible en un tamaño de envase de 195 viales (1.170 dosis) y puede almacenarse a 2-8°C hasta un mes).
"Estas diferencias proporcionarán mejores opciones de almacenamiento, transporte y logística para la distribución y administración de la vacuna. La nueva formulación estará disponible en un despliegue gradual que comenzará a principios de 2022", ha explicado la EMA en un comunicado.